作者信息
通讯作者:于学来
中国科学院大学附属肿瘤医院(浙江省肿瘤医院)麻醉科
其他作者:吴庭豪 龚昌盛 蒋飞 卜叶波
新青年麻醉论坛病例版

药物滥用是全球性的公共卫生问题,截至2018年底全国现有吸毒人员240.4万名。由于毒品来源、种类和吸毒人数不断扩大,需要手术治疗疾病的吸毒患者也随之增加。2017年全球因吸毒死亡的58.5万人中,2/3是由阿片类药物导致的,阿片类依赖性强,极易成瘾。
本文主要回顾阿片类物质成瘾患者的围术期管理(部分内容涉及其他毒品)。
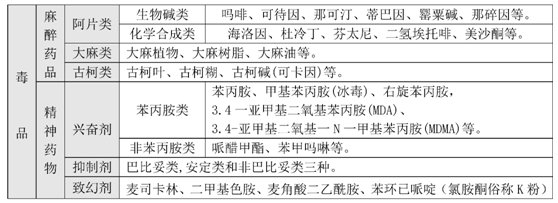
表1 国家规定管制的毒品简要分类
一、术前访视
(一)术前检查
1. 实验室检查
(1)常规检查:血常规、生化、凝血、心电图、以及传染病筛查;
(2)吸毒相关检查:阿片类物质生物学检测、尿检分析、必要时进行戒断实验、相关心理学量表评估等,有助于全面了解病人状态。
2.其他特殊检查
(1)心电图如有异常应行进一步行胸片、心肌酶谱、动态心电图监测、心脏超声检查;
(2)毒品中所含杂质及长期注射毒品造成的静脉壁受损使患者血栓形成风险增高。D-二聚体筛查有助于排查血栓,必要时行超声检查,高危患者预防性抗凝治疗;
(二)术前准备:
(1)营养及精神状态:吸毒患者并存营养不良及精神疾病的风险增加,应及时营养支持和心理干预减轻术前焦虑和抑郁水平。
(2)术前药物:
①给予咪达唑仑、氯胺酮、东莨菪碱等镇静、镇痛、抗胆碱药物便于麻醉管理。东莨菪碱具有抑制腺体分泌、镇静、拮抗迷走神经效应的作用,防止术中毒瘾发作时分泌物剧增来确保呼吸道清洁可作为首选。盐酸戊乙奎醚(长托宁)作为胆碱能受体(M1、M3)阻滞剂可以抑制腺体分泌的同时不增加心脏交感神经兴奋作用,与氯胺酮联合使用具有较好效果。
②术前需要镇痛药物维持的患者应维持日常剂量到手术当天。
③非法使用阿片物质患者替代药物的选择:μ-阿片类受体激动剂,推荐吗啡,氢吗啡酮,芬太尼或舒芬太尼,静脉滴定给药控制症状,需严密监测其副反应;美沙酮是合成的阿片受体激动剂及NMDA受体拮抗剂,消除半衰期平均24-36h,术前已经开始替代治疗沿用原有治疗。首次用药者,初始剂量,30-40mg,1次/天。滴定剂量,出现撤药症状,口服每30-45min按需追加10mg,静脉每10min追加0.5-1mg,评估有效性按需调整剂量。
(三)评估要点:
1. 吸毒相关评估
吸毒时间、吸毒方式、毒品种类、使用频率和剂量,特别是近期内阿片物质使用与治疗情况,是否发生过戒断反应。
吸毒患者临床表现因个体差异、毒品种类、吸毒途径和阶段而异(见表2)。
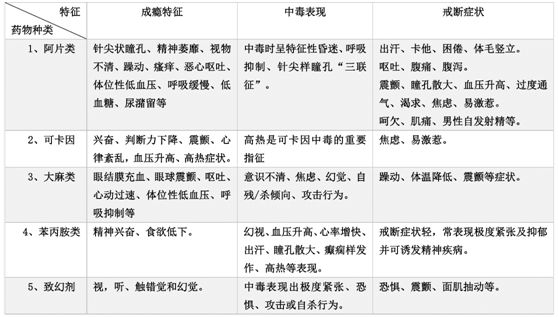
表2 常见5类毒品药物成瘾特征、中毒表现及戒断症状
2.器官受累评估
(1)心血管系统:毒品中所含混杂物质可引起感染性心内膜炎、瓣膜炎性赘生物、缺血性心肌病和心肌中毒,导致肺动脉高压、肺源性心脏病、肺栓塞。心肌酶可反映近期心肌缺血情况;心电图可反映心肌缺血和梗死情况;心脏超声可评估心功能及瓣膜情况。
(2)肝脏;是否存在病毒性和非病毒性肝炎,肝功能及凝血情况。
(3) 肾脏:长期应用吗啡能引起肾上腺增生和皮质类固醇分泌功能的损害。肾功能、激素测定均有助于评估。
(4)躯体:四肢是否有注射瘢痕,皮肤脓肿、蜂窝织炎,脊椎有无感染、压痛及外伤史。
3.传染病防治
2017年,全球有数百万人注射毒品,其中140万人感染艾滋病毒,560万人患有丙型肝炎。吸毒者多为艾滋病、肝炎、梅毒、淋病等传染性疾病的高危和高发病人群。行产前检查和传染病筛查,能及时阻断传染病母婴传播。合并感染HIV病人,要及时转到艾滋病治疗机构接受规范治疗。医务人员自身应从各个环节加强自我保护,预防职业暴露的发生。
毒品成瘾是多种神经递质参与的慢性复发性脑疾病,亦是心理疾病。此类患者多为外伤、妇产科等急诊手术,一般抵触诉说吸毒史,术前访视需要综合运用精神科病史采集技巧和成瘾疾病知识,采用非歧视的态度向患者及家属阐明利害关系,详细了解其病史。
二、麻醉期间管理
(一)麻醉方案
1. 麻醉方式选择:
(1)椎管内及神经阻滞麻醉:
椎管内麻醉发生毒品复吸风险低。但椎管内麻醉后低血压发生率增加,而且体内β-内啡肽浓度显著升高,易诱发戒断症状。另外穿刺部位感染、凝血功能障碍、脓毒症、可卡因引起的血小板减少、海洛因依赖引起骶髂关节感染等应被视为腰部硬膜外麻醉的禁忌。
神经阻滞麻醉安全可行,但有报道神经阻滞麻醉需要追加镇痛处理,这与阿片药物诱导的疼痛异常敏感学说一致。推测可能与β-内啡肽水平的异常及μ、κ阿片受体密度的慢性变化有关。
椎管内麻醉、区域神经阻滞麻醉和局部麻醉均需患者充分合作。吸毒患者免疫功能低下,感染发生率高,需格外注意无菌操作,出现神经感染的任何症状均需紧急评估。
(2)全身麻醉:
全麻的镇静、镇痛、遗忘、肌松作用有助于控制气道、预防和控制戒断症状。对于合作不佳的患者,全身麻醉更为适宜。但是由于吸毒者对阿片类药物具有耐受性和交叉耐受性以及痛觉过敏(痛阈降低),所以镇痛药物剂量范围大,出现镇痛不足、戒断症状及复吸风险增加。
麻醉方案需充分考虑手术方式以及患者配合程度和可控性,联合麻醉可优势互补、减少不良反应,我们应个体化治疗来保证医疗安全。
2. 麻醉药物的选择
(1)吸入麻醉药:
短时间内摄入苯丙胺可增加吸入药物的最低肺泡有效浓度,而长期摄入可能减少对全麻药物的需求。长期可卡因滥用的患者应尽量避免使用氟烷、异氟醚以减少心血管的毒性作用。
(2)静脉镇静药物:
①苯二氮卓类药物具有镇静、催眠、抗焦虑、抗惊厥(抗癫痫)以及肌肉松弛等作用。因起效快、疗效确切、短期使用耐受性好、顺行性遗忘的特点可以应用于吸毒患者;
②依托咪酯由于对控制锥体外系中枢神经有部分的去抑制作用,导致肌肉痉挛、癫痫发作、反射亢进,需要谨慎使用;相比之下丙泊酚是安全有效的。
③α2肾上腺素能受体激动剂(右美托咪定、可乐定)不仅能治疗戒断反应,而且能作用于脊髓胆碱能中间神经上的受体,抑制兴奋性递质和伤害感受性肽类的释放参与镇痛,还能作用于蓝斑核、额叶皮层的受体,产生镇静、抗焦虑作用。
(3)镇痛类药物:阿片药物应个体化剂量。①使用瑞芬太尼要考虑术后痛觉过敏的发生情况,建议应用瑞芬太尼时应及时使用长效阿片类药物进行桥接避免术后痛觉过敏和戒断反应的发生;②氯胺酮的镇静、镇痛、选择性网状结构的上行传导阻滞作用有利于戒断症状治疗。麻醉中或术后辅以氯胺酮,对治疗戒断症状,完善麻醉和镇痛均有益处,故在处理此类患者麻醉时,氯胺酮是较好的选择。
(4)肌松药物:琥珀酰胆碱应用后肌肉束颤及肌张力增高影响戒断反应的判断应慎用,如需快速建立气道可选择罗库溴铵。肝肾功能异常患者选择顺式阿曲库铵较佳。
(5)局麻药品:需要注意毒品与局麻药的相互作用使局麻药的安全剂量难以估算。吸食可待因类患者应避免应用酯类局麻药,使用时需降低局麻药的总量减少心脏毒性。
(6)拮抗药物:避免拮抗以免干扰复苏期戒断反应的判断。慎用纳洛酮及氟马西尼以避免产生戒断应激。若患者存在呼吸缓慢或呼吸抑制,可予非特异性的呼吸兴奋剂多沙普仑进行拮抗。苏醒延迟需排查阿片药物中毒等因素。
(7)抢救药物:吸毒患者血管收缩、血容量下降,易出现低血压。长期吸食可卡因者神经末梢内去甲肾上腺素释放殆尽,对麻黄碱及阿托品效果多不明显,因此充分扩容较为必要,升压药物可以考虑去氧/去甲肾上腺素。
(8)其他辅助药物:
①右旋氯胺酮:减少痛觉过敏,改善阿片类药物耐受,单次负荷量0.25-0.5mg/kg,术中及术后持续静脉输注,1-2ug/kg/min。
②三环抗抑郁药物(TCA):阻断去甲肾上腺素能神经末梢再摄取,降低突触前膜α2受体的敏感性,阻断5-羟色胺能神经末梢的再摄取,常用药物:阿米替林或多塞平(10-20mg qn)。
③抗惊厥药物:辅助镇痛以降低阿片药物用量,减轻焦虑,预防慢性持续性疼痛,用法:加巴喷丁1200mg,术前;普瑞巴林300mg,术前用,随后150mg bid 连续应用数天。
④COX-2抑制剂:减少脊髓兴奋性神经递质释放,与NMD受体拮抗剂发挥协同作用。
⑤曲马多通过激动中枢阿片类受体和抑制中枢单胺能物质(5-羟色胺和去甲肾上腺素)的再摄取而发挥镇痛效应,长期使用曲马多可产生药物依赖作用。对于吸毒患者术后是否采用该镇痛仍有争论。
吸毒患者对中枢镇静、镇痛药均有一定的耐受性。综合评估对剂量进行调节,联合用药完善镇痛的同时来降低戒断反应和复吸风险。
(二)术中监测
1.标准的麻醉监测:包括血压、心电图、脉搏血氧饱和度、呼气末二氧化碳以及体温。视手术情况行尿量、血气、血糖监测;
2.血流动力学监测:戒毒3个月以上,循环相对平稳,但戒毒2周内手术麻醉,术中血流动力学波动较大。吸毒患者不仅常伴有严重的血管收缩和血容量不足,而且戒毒治疗所用药物具有镇静、降压的作用,可导致围术期血流动力学的剧烈变化。建议对有心肺基础疾病、手术范围较大、对生理状态影响大的手术行中心静脉穿刺来监测CVP、快速补液、泵注血管活性药物,动脉置管监测有创动脉血压及基于有创动脉压的循环血容量监测。
3.麻醉深度监测:吸毒患者术中知晓发生率显著增高。BIS、听觉诱发电位监测对此类患者更为必要。如有条件进行镇痛监测可以指导药物的应用。
吸毒患者麻醉中监测除了常规监测外,应加强麻醉深度和血流动力学的监测,防止术中知晓和血流动力学波动的发生。
(三)术中管理
1.特殊情况的麻醉管理:
(1)采用大剂量纳洛酮或纳曲酮用作阿片物质成瘾的治疗时:给予阿片拮抗剂前需全麻诱导,同时需要一定深度的麻醉维持以防止患者突然出现戒断症状,对阿片成瘾患者,应用纳洛酮(总剂量12.4mg)阻断阿片受体后可导致交感神经兴奋,包括血浆儿茶酚胺浓度增高以及心血管刺激,可用α2肾上腺素受体激动剂加以阻断。
(2)处于纳曲酮治疗期间:大剂量的阿片类物质可以反转纳曲酮的作用,同时也会出现阿片类物质过量的风险;停用纳曲酮缓释注射剂治疗的患者对阿片类物质的耐受性降低,使用与既往同样甚至更低剂量的阿片类物质可导致过量中毒。文献提示在长效纳曲酮应用的患者中发现肌松药代谢增快,推测与全麻药物的耐受造成协同作用降低有关。
(3)吸毒患者产科麻醉管理:
孕产妇的影响:使用海洛因的妊娠女性,产科并发症增加6倍,包括宫内生长受限、妊娠晚期阴道出血、先露异常、早产和胎儿不稳定。
对胎儿的影响:所有阿片类药物均能自由通过胎盘。目前没有发现特定的胎儿先天畸形与慢性阿片类药物滥用有关,但死产、胎粪污染、头围减少和 Apgar评分下降的风险增加。胎儿期暴露于海洛因的新生儿中有50%-95%出现戒断综合征。新生儿戒断症状与成人相似,同时还有易激惹、吸奶无力,严重者发生癫痫,甚至死亡。母亲滥用氢化吗啡酮或羟考酮后,新生儿也会出现戒断症状。对于母亲戒毒时间较短的新生儿,亦应严密观察,制定相应预案。新生儿戒断综合征一般不用药物治疗也可自行缓解,戒断症状持续不缓解或日趋严重时需给予药物(丁丙诺啡)治疗。
麻醉管理中需要考虑阿片类诱导的痛觉过敏、镇痛药物耐受增加、依赖性诱发的戒断反应等。术中不仅要求麻醉平稳、提供充分镇痛,同时要有效控制戒断症状及防止发生复吸或精神依赖加重。
三、术后管理
(一)术后镇痛及疼痛管理:
1.术后镇痛:术后镇痛可采用切口浸润、神经阻滞、静脉/硬膜外自控镇痛。药物可选用布比卡因或罗哌卡因和氯胺酮,静脉自控镇痛药物可选用非甾体抗炎药氯诺昔康和氯胺酮。
2.阿片类药物依赖患者急性疼痛管理目标:①防治戒断反应和并发症;②对心理情感障碍如焦虑等对症治疗;③在急性期进行有效的镇痛治疗;④使其复原到可接受且合适的阿片维持状态。
3.日常处于药物维持过程患者的疼痛治疗方法:①继续服用原药物维持剂量的美沙酮(为安全起见可分次服用);②评估疼痛级别和镇痛效果,以确定用药剂量;③最好选用其它阿片类药物(吗啡、羟考酮等);④禁止使用激动拮抗剂类药物;⑤可使用非阿片类镇痛药物作为补充。
由于阿片药物导致的痛觉过敏及中枢系统对疼痛刺激的过度反应,对疼痛低估和处理不足在这类患者中很常见,及时评估效果和个体化调整镇痛方案。
(二)术后并发症处理:
1. 急性中毒:需排除如外伤、感染等所致的急性意识障碍。
(1)病因:使用大剂量阿片类药物或者患者对阿片类药物耐受下降、合并其他物质(多药)使用、缓解戒断症状而补偿性超量均可导致急性中毒。
(2)临床表现:典型的临床“三联征”表现为昏迷、针尖样瞳孔和呼吸抑制(呼吸节律变慢、深度变浅,严重时可降至2~4次/分钟)。其它表现有皮肤湿冷、体温降低、紫绀、肺水肿、心律减慢、休克、下颌松弛及舌后坠等。
(3)治疗方法:
一般治疗措施:①监护生命体征、维持呼吸道通畅,确保有效供氧,必要时呼吸支持;②建立双路静脉给药通道,保证纳洛酮维持的同时另一路进行呼吸、循环衰竭的救治;③定期进行动脉血气和生化检查,维持水、电解质和酸碱平衡,保持足够尿量,注意保暖;④对伴有低血压、心动过缓、非心源性肺水肿和颅内压升高患者,应及时对症处理,以防止病情加重;⑤病情平稳后,还应持续监护意识状态、体征和心肺功能变化24h以上,以防止发生意外。
阿片受体特异性拮抗剂是抢救阿片类物质急性中毒的关键,要尽早、及时、足量和足疗程使用。当纳洛酮使用注意超过20mg无效时,应考虑诊断是否正确,是否还合并有缺氧、缺血性脑损伤、其它药品或毒品中毒,如合并大剂量镇静催眠药中毒昏迷者纳洛酮无效;纳洛酮可能诱发戒断症状,部分患者可出现谵妄、躁动,应给予重视和加强护理。
可卡因类、大麻类、苯丙胺类、致幻剂类无特殊解毒治疗方法,以对症支持治疗为主。
2.急性戒断反应:
(1)病因:有反复、长期和/或大剂量使用阿片类物质病史,停止或减少用量时出现急性戒断症状;使用阿片受体拮抗剂或阿片受体部分激动剂后诱发。
(2)临床表现:(见表2)戒断反应以胆碱能神经和去甲肾上腺能神经兴奋,以及其他神经递质大量释放为主要特征。表现为心血管应激等围术期应激症状。严重程度和持续时间和种类、剂量、半衰期、停药方式和是否拮抗相关。围术期注意排除由于医源性镇痛不足等原因导致的假性成瘾。
(3)发作时间:通常为所戒断阿片类物质的2-3倍半衰期。静脉使用芬太尼后戒断症状出现在停药后3-5h出现,高峰期在8-12h,持续4-5d。短效类(如吗啡、海洛因)戒断症状一般在停药后8-12h出现,高峰期在48-72h,持续7-10d。长效类(如美沙酮)戒断症状出现在停药后1-3d,高峰期在3-8d,可持续数周。使用拮抗剂(如纳洛酮或纳曲酮)后戒断症状可即刻出现,持续数小时到1d,并且比自发戒断症状严重。
(4)治疗方法:戒断症状防治以通过继续应用阿片类药物或替代治疗的方式,以维持稳定的药物依赖状态,控制症状为原则。
①首选氯胺酮2.0mg/kg,其为N-甲基-D-天冬氨酸受体的非特异性拮抗剂,具有镇痛、遗忘、保护脑细胞以及抗炎作用与阿片受体、胆碱能受体、单胺受体等结合共同产生镇痛作用,有效对抗戒断症状。
②α-肾上腺素能受体激动剂不仅能抑制戒断反应,还有镇静镇痛抗焦虑作用。可乐定通过用α2受体激动作用介导的CNS抑制作用替代阿片类药物的抑制作用,从而减轻戒断症状。
当出现不明原因的心律失常、呼吸急促等应考虑戒断症状。若无禁忌证控制戒断症状首选氯胺酮联合应用咪达唑仑、丙泊酚等镇静催眠药,保证呼吸道通畅,辅以抗精神病药物,加强监护并缓慢减药。
吸毒患者的疼痛治疗及麻醉管理给我们提出了较大挑战,围术期应制定清晰明确的麻醉方案和多模式的疼痛管理计划,保证医疗安全,使吸毒患者平稳安全的度过围术期。
参考文献
[1]《2018年中国毒品形势报告》《2019年世界毒品问题报告》
[2]阿片类物质使用相关障碍诊断治疗指导原则[J]. 中国药物滥用防治杂志, 2017(1).
[3]Alan C.Santos, Jonathan N.Epstein, Kallol Chaudhuri. 临床麻醉学指南产科麻醉(Obstetric Anesthesia). 陈新忠,黄绍强,张鸿飞,译.北京:北京大学医学出版社, 2017:237-244.
[4]赵国胜. 纳曲酮长效缓释剂皮埋患者行腹腔镜监护下宫腔镜探查术麻醉一例[J]. 临床麻醉学杂志, 2014, 30(3):310-310.
[5]钱自亮, 吕洪城, 朱木棕. 吸毒患者的麻醉处理[J]. 临床麻醉学杂志, 2001(2).
[6]赵继蓉, 陈峰, 吴娟.吸毒产妇剖宫产手术麻醉一例[J]. 上海医学, 2013(10):910-910.
[7]苏永军, 方惠, 王燕. 吸毒患者12例麻醉体会[J]. 临床军医杂志, 2009, 37(6):1018-1018.
[8]柳培雨, 田毅. 常见吸毒患者的临床麻醉处理[J]. 医学与哲学(临床决策论坛版), 2011, 32(8):43-44.
[9]中华人民共和国国家卫生和计划生育委员会. 阿片类物质使用相关障碍诊断治疗指导原则[J]. 中国实用乡村医生杂志, 2018(4):5-11.
[10]Ludlow J , Chrislmas L , Paech M J , et al. Drug Abuse and Dependency during Pregnancy: Anaesthetic Issues[J]. Anaesthesia and intensive care, 2007, 35(6):881-893.
[11]Weiss F , Ciccocioppo R , Parsons L H , et al. Compulsive drug-seeking behavior and relapse: Neuroadaptation, stress, and conditioning factors[J]. Annals of the New York Academy of Sciences, 2001, 937:1-26.
[12]Vocci F J , Acri J , Elkashef A . Medication Development for Addictive Disorders: The State of the Science[J]. American Journal of Psychiatry, 2005, 162(8):1432-1440.
[13]Meehan T J , Bryant S M , Aks S E . Drugs of Abuse: The Highs and Lows of Altered Mental States in the Emergency Department[J]. Emergency Medicine Clinics of North America, 2010, 28(3):663-682.
[14]Hernandez M , Birnbach D J , Van Zundert, André AJ. Anesthetic management of the illicit-substance-using patient[J]. Current Opinion in Anaesthesiology, 2005, 18(3):315-324.
[15]Smith D H , Bruckenthal P . Implications of Opioid Analgesia for Medically Complicated Patients[J]. Drugs & Aging, 2010, 27(5):417-433.
[16]Adams H A , Werner C . Vom Razemat zum Eutomer: (S)-Ketamin Renaissance einer Substanz?[J]. Der Anaesthesist, 1997, 46(12):1026-1042.
[17]Kuczkowski K M . Anesthetic implications of drug abuse in pregnancy.[J]. Journal of Clinical Anesthesia, 2003, 15(5):382-394.
[18]刘芳, 段宏军, 邹德成. 吸毒患者围术期麻醉处理的探讨[J]. 中国临床医生杂志, 2003, 31(4):29-30.
[19]仓静教授于2019年中国医疗保健国际交流促进会 区域麻醉与疼痛医学分会学术年会上关于吸毒患者麻醉管理的报告

声明
本微信公众号所刊载原创或转载内容不代表新青年麻醉论坛观点或立场。文中所涉及药物使用、疾病诊疗等内容仅供参考。

在看点这里