
糖尿病治疗的最终目的,是预防并发症,改善患者生活质量!
美国糖尿病学会(ADA)在其2019年指南中写道:2型糖尿病(T2DM)治疗的终极目标,是预防糖尿病并发症,改善患者生活质量[1]。
从单纯强化降糖变革为降糖、降压、调脂的综合管理,逐渐被各个研究证实具有降低T2DM患者微血管并发症风险的作用,也写入了指南[1,2],应用于临床实践。然而,作为T2DM患者致死致残主要原因的并发症——心血管并发症,降糖本身及传统的降糖药物还缺乏强力的获益证据。
T2DM管理遭遇瓶颈,这一切如何“变局”与“突破”?在全球医药研发领域,有一位传奇人物,一直致力于糖尿病治疗药物的开发,他先后研发了格列喹酮、瑞格列奈、利格列汀以及最近炙手可热的钠葡萄糖协同转运蛋白2抑制剂(SGLT2i)恩格列净。正是由于他的贡献,2019年他被世界心脏联盟评为全球“心脏英雄”!这位心脏英雄,就是德国勃林格殷格翰公司心血管和代谢疾病研究的副总裁和全球负责人Michael Mark博士。今年的世界心脏日之际,Michael Mark博士来到中国,与中国内分泌医生和药师面对面交流,介绍恩格列净研发背后的故事,更呼吁重视T2DM患者的心血管疾病风险。

Michael Mark博士获得全球“心脏英雄”称号
(图片源自世界心脏联盟网站)
1两个启示,“孕育”出SGLT2抑制剂
早在1835年,法国化学家从苹果树皮中提取了根皮苷[3],当时认为根皮苷可用于治疗发热、 感染性疾病及疟疾,后来发现大剂量根皮苷可引起葡萄糖尿。动物实验证实,根皮苷可使90%胰腺切除的糖尿病大鼠出现葡萄糖尿,使其空腹和餐后血糖恢复正常,逆转第一、第二时相胰岛素分泌缺陷和胰岛素抵抗[4]。随着葡萄糖协同转运蛋白(SGLT)的发现,人们认识到肾脏葡萄糖重吸收的90%由位于近端小管S1、S2段刷状缘膜的SGLT2完成,而这种效应可作为降糖作用的一种潜在的机制。
另一个启示来自家族性肾性糖尿(FRG)。FRG是一种常染色体隐性遗传病,患者SGLT2缺陷导致肾小管对葡萄糖的转运功能受损,从而使大量葡萄糖从肾脏丢失,多数患者无症状,预后较好[5]。由此及彼,研究者受到启示,逐步开发出多种抑制SGLT2的药物,通过减少葡萄糖在肾小管的重吸收促进尿糖排泄,最终达到降低血糖的目的[5]。
恩格列净是一个强效、高选择性的SGLT2i,单药治疗24周,减去最大安慰剂效应后可使HbA1c下降0.74%,高基线患者HbA1c下降更高达1.45%,体重也较安慰剂显著下降高达2kg,总体安全性和耐受性良好[6]。
2恩格列净:背水一战终成名
2007年,荟萃分析发现罗格列酮较安慰剂显著增加心肌梗死风险,而心血管死亡风险的增加也达到了有统计学差异的临界值,这一发现引发人们对降糖药物心血管安全性的关注[7]。随后,美国食品药品监督管理局(FDA)要求对上市的新型降糖药物必须在心血管高危人群中进行以心血管事件为终点且随访不少于2年的临床研究,即心血管结局研究(CVOT)[8]。作为新型降糖药物,SGLT2i类药物也必须开展CVOT,在评价其心血管安全性后方可上市。
作为全球第三个上市的SGLT2i,恩格列净仅在上市第二年(2015年)就公布了震惊业界EMPA-REG OUTCOME结果。而其它SGLT2i的CVOT直到2017年才陆续发布。为什么恩格会抢跑这么多?
回溯到药物开发初期,除了知道恩格列净具有降糖、降压、减重的作用外,Michael Mark博士带领的研发团队对其心血管安全性一无所知。开展CVOT需要投入大量资金,如果获得不满意的结果等于功亏一篑。是背水一战,大胆冒险,还是果断放弃?最终,德国勃林格殷格翰公司投入数巨额资金开展了EMPA-REG OUTCOME研究,并一战成名——恩格列净成为首个获得证实具有心血管明确获益的SGLT2i。


Michael Mark博士正在与国内专家讨论
研究结果显示,与安慰剂相比,恩格列净显著降低合并心血管疾病的T2DM患者非致死性卒中、心肌梗死和心血管死亡的复合终点(3P-MACE)风险达14%,同时使心血管死亡风险显著降低38%,使全因死亡风险和心衰住院风险分别显著降低32%和35%[9]。其机制可能与恩格列净利尿、改善血流动力学、改善能量代谢等作用有关[10,11]。
那么,SGLT2i的心血管保护是否是类似效应?在恩格列净、达格列净和卡格列净的CVOT中,它们都能显著降低心衰住院风险和肾脏事件[9,12,13],但仅仅恩格列净的研究结果在降低3P-MACE风险、心血管死亡风险上同时达到了优效结果[9](图1)。

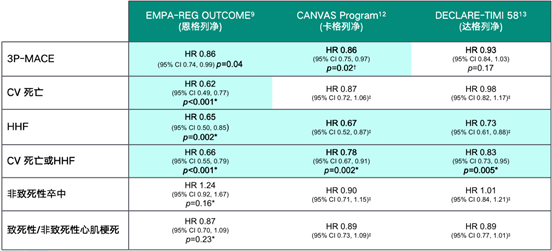
图1 三种SGLT2i心血管安全性研究结果比较(颜色标记的为达到显著性下降)
3 降糖“专一”才放心
SGLT家族主要包括SGLT1-SGLT6,在体内广泛分布[14](图3)。其中SGLT2主要主要表达于近曲小管S1节段处,SGLT1主要表达于小肠刷状缘和肾近曲小管的S3节段中[17]。有观点认为,SGLT1/SGLT2双抑制剂可抑制肠道葡萄糖、乳糖的吸收,将带来更好的降糖效应。在已经上市的SGLT2i中,仅有300mg卡格列净可以同时抑制SGLT1和SGLT2,但中国没有此规格,而300mg卡格列净也未带来血糖的进一步下降。
表1 SGLT家族的分布及功能[15-16]

SGLT2i的远祖根皮苷之所以不能作为治疗糖尿病的药物,主要原因是其对SGLT1和SGLT2的抑制作用缺乏选择性。抑制分布在小肠、心肌细胞中的SGLT1后,很容易引起包括腹泻和脱水在内的胃肠道不良事件,也可能影响心肌细胞对葡萄糖的摄取(尤其是心肌缺血缺氧时)[18,19]。同样,SGLT1/SGLT2双抑制剂Sotagliflozin也未表现出降糖及心肾变化方面的优势,在2型糖尿病适应证开发失败,相关公司的开发和商业化合作因此终止。
与卡格列净、达格列净相比,恩格列净对靶点蛋白SGLT2抑制作用选择性更强更“专一”。3种SGLT2i中,恩格列净对SGLT2选择性最高,分别是达格列净的2倍,是卡格列净的10倍[19]。高选择性SGLT2i恩格列净可能拥有更好的胃肠道耐受性,有效减少“脱靶效应”,保障用药安全。
总 结
恩格列净是强效、高选择性的SGLT2i,除了降糖、减重等作用,也能带来明确的心血管获益,总体安全性良好。对于合并冠状动脉粥样硬化性心血管疾病(ASCVD)或慢性肾脏病的T2DM患者,恩格列净等SGLT2抑制剂已被2019年ADA指南推荐用于降糖治疗的优选药物[1],ESC/EASD《糖尿病/糖尿病前期和心血管疾病指南》也推荐合并ASCVD或心血管高危/极高危的T2DM患者将恩格列净等SGLT2i作为一线降糖治疗(Ⅰ类,A级),恩格列净也是该指南唯一推荐用于合并心血管疾病的T2DM以降低死亡风险(Ⅰ类,B级)的降糖药物[20]。至此,恩格列净俨然已成为T2DM的“变局者”,助力T2DM管理取得新突破。
